
文丨云潭
中国创新药产业正从技术跟随迈向全球领跑,肿瘤免疫治疗领域迎来新一轮技术革命。当PD-1/PD-L1单抗进入疗效瓶颈期,双特异性抗体技术成为突破口:康方生物AK112(PD-1/VEGF双抗)在头对头研究中击败K药,信达生物IBI363(PD-1/IL2双抗)则展示了激动剂双抗在延长生存期方面的优势。行业目光聚焦于兼具疗效、安全性和广谱适应症的下一代基石药物,维立志博自主研发的PD-L1/4-1BB双抗LBL-024(奥帕替苏米单抗)正成为这一领域的标杆。
【冷肿瘤克星:全球首个4-1BB靶向双抗】
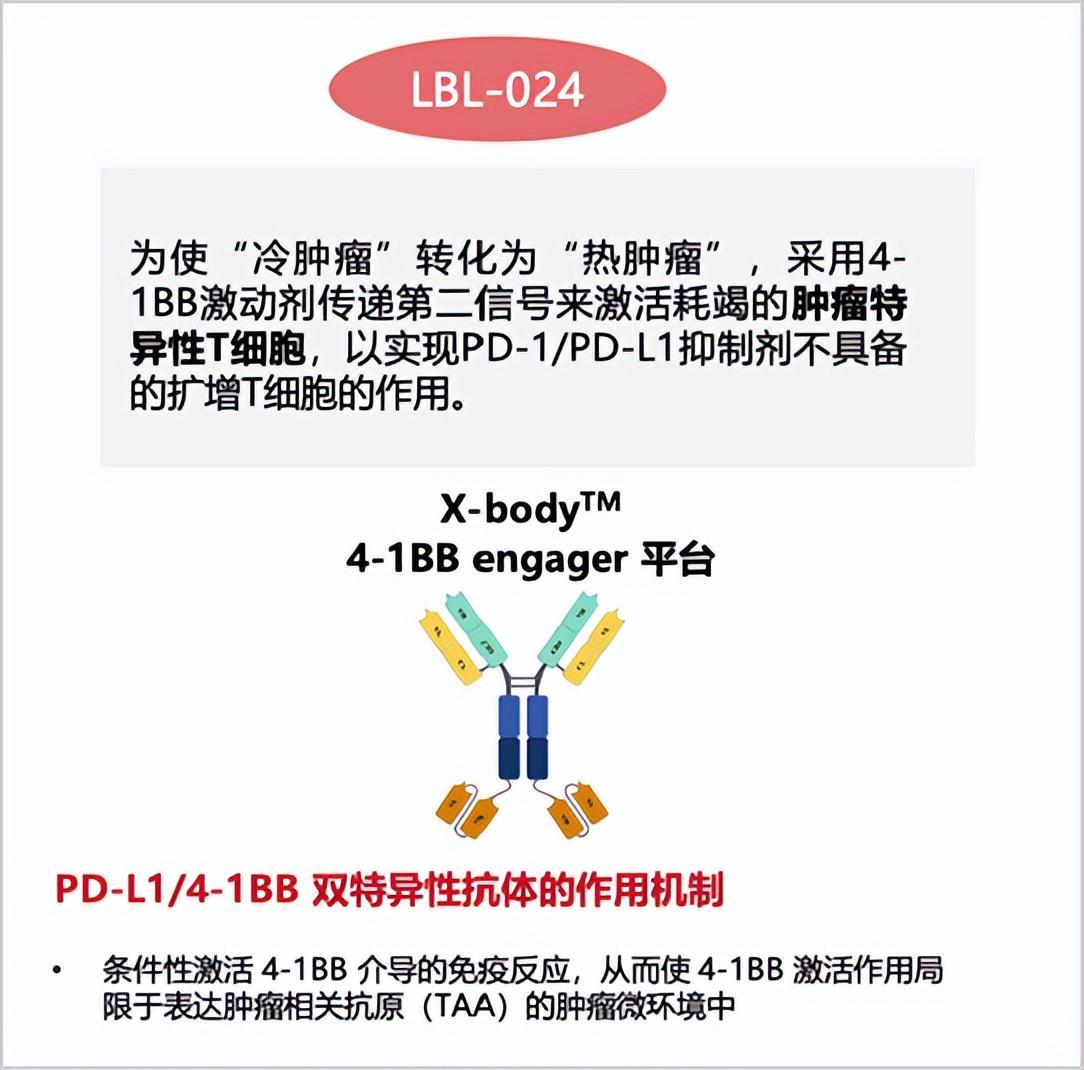
作为全球首个进入关键注册临床阶段的4-1BB靶向药物,LBL-024自2025年7月维立志博登陆香港资本市场以来备受关注。该药物基于企业自主研发的X-body®平台开发,通过同时靶向PD-L1与4-1BB两个免疫检查点,直击传统PD-1/PD-L1单抗的核心痛点——仅20%左右的应答率和易产生的耐药性。
传统PD-1/PD-L1疗法通过恢复T细胞功能发挥作用,但无法解决T细胞数量不足的问题。LBL-024创新性引入4-1BB激动剂,如同为免疫系统注入"魔法子弹":既能重新激活凋亡的T细胞,又可将其数量从几十个扩增至数万个,形成持续抗癌能力。在肺外神经内分泌癌、小细胞肺癌、胆道癌等冷肿瘤的临床试验中,该药物展现出远超传统疗法的疗效,显著延长患者生存期。
【技术突破:条件激活破解安全性难题】
4-1BB靶点的研究可追溯至1989年,但此前辉瑞、BMS等跨国药企的临床试验均因全身性激活导致的严重肝毒性而折戟。维立志博通过双抗的靶向机制实现条件激活:仅在表达PD-L1的肿瘤微环境中激活4-1BB,既保证疗效又降低毒性。在400余例入组患者的临床试验中,未发生剂量限制性毒性事件,安全性与PD-1/PD-L1单抗相当。
从作用机制看,PD-L1抗体解除免疫抑制(松刹车),4-1BB激动剂激活T细胞(踩油门),二者协同形成"双引擎"治疗方案。在肺外神经内分泌癌领域,北京大学肿瘤医院沈琳教授牵头的I/IIa期临床显示:后线单药治疗中位总生存期(mOS)达现有疗法两倍,一线联合化疗客观缓解率(ORR)达83.3%,疾病控制率(DCR)达100%,创下该领域治疗纪录。
【临床进展:多癌种布局显商业价值】
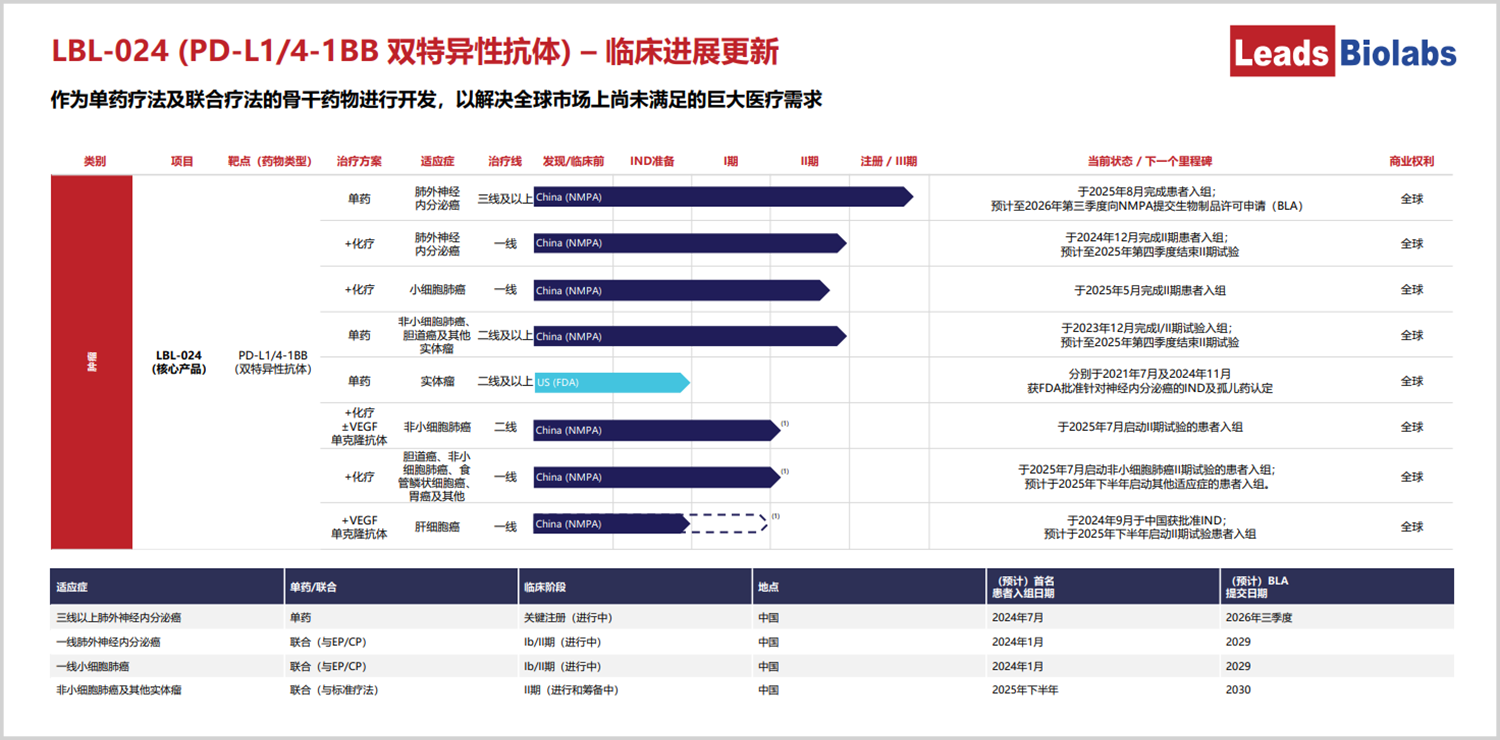
LBL-024的临床开发呈现"单点突破到全面覆盖"的特征。除肺外神经内分泌癌外,该药物已在小细胞肺癌、非小细胞肺癌、胆道癌、肝癌、黑色素瘤、卵巢癌和三阴性乳腺癌等8大癌种展开布局。其中,一线小细胞肺癌II期临床试验联合化疗取得86.5%的ORR和96.2%的DCR,中山大学肿瘤防治中心张力教授牵头的非小细胞肺癌研究正快速推进。
凭借显著疗效,LBL-024提前4个月完成肺外神经内分泌癌关键注册临床试验患者入组,并获得中美监管双重认证:中国药监局授予突破性疗法认定,FDA授予孤儿药资格。这意味着该药物有望成为全球首个针对肺外神经内分泌癌的获批药物,更是4-1BB靶点在全球范围内的首次成药。
【市场前景:千亿赛道的领跑者】
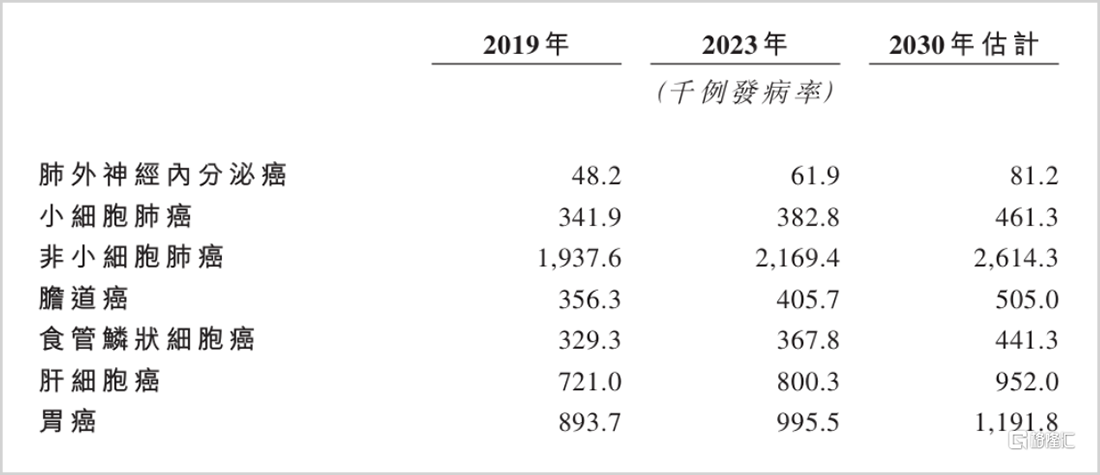
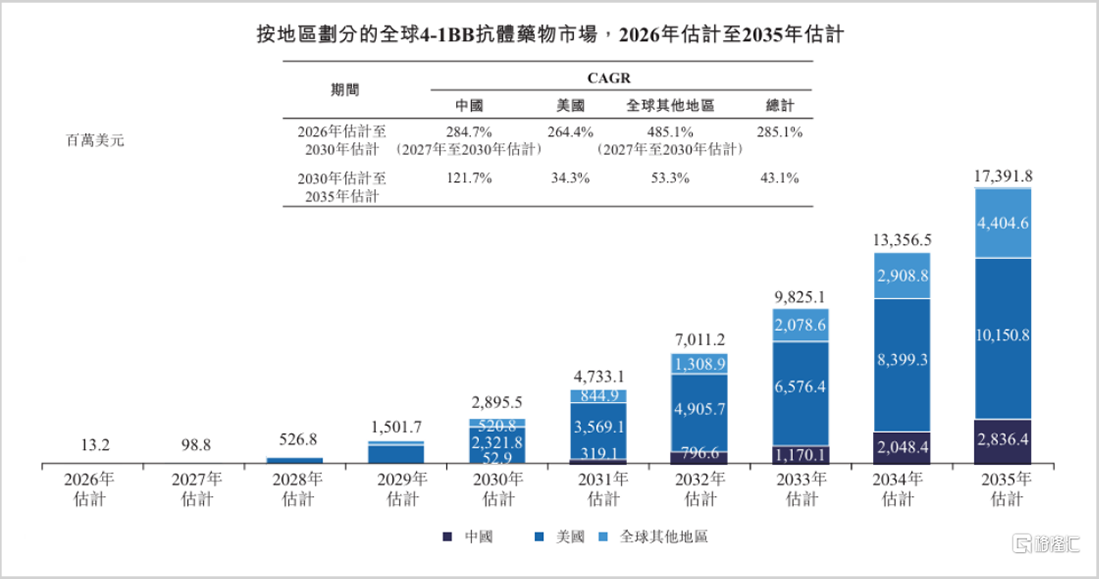
弗若斯特沙利文预测,全球4-1BB抗体市场到2035年将达174亿美元。LBL-024不仅瞄准肺外神经内分泌癌(到2030年发病率超8万例),更覆盖小细胞肺癌(46万例)、非小细胞肺癌(260万例)等庞大市场。其广谱潜力与高安全性特征,使其在ADC+IO联合治疗战略中具有独特优势,可与多种疗法联用提升整体疗效。
该药物预计2026年第三季度提交生物制品许可申请(BLA),2027年有望获批上市。作为维立志博商业化的核心资产,LBL-024将推动企业从研发型向综合型药企转型。当前,A股科技股牛市与H股创新药板块走强形成共振,维立志博凭借first-in-class药物研发策略,正获得资本市场高度关注。
回望肿瘤免疫治疗发展史,2014年PD-1单抗的诞生开启了IO 1.0时代。如今,LBL-024代表的IO 2.0技术正重塑治疗格局。作为继CTLA-4、PD-1/PD-L1、LAG3之后第四个成功成药的免疫检查点,该药物若成功上市,不仅将为中国创新药增添重磅产品,更可能重新定义全球肿瘤治疗标准。
免责声明
本文涉及上市公司的内容基于企业公开披露信息分析,不构成投资建议。市场有风险,决策需谨慎。
